Sınıf:
Ünite:

Asitler ve Bazlar
Asitlerin Genel Özellikleri
- Suda çözündüklerinde suya hidrojen (H+) iyonu veren maddelere asit adı verilir.
- Tatları ekşidir.
- Birçoğu yakıcı ve tahriş edicidir. Canlı dokulara zarar verir.
- Bazı metallerle (Mg, Cu, Zn gibi) tepkimeye girerek metalleri de aşındırır.
- Mermeri aşındırır.
- Mavi turnusol kâğıdını kırmızıya dönüştürür.
- Sulu çözeltileri elektriği iyi iletir.
- Bazlarla tepkimeye girerek tuz ve su oluşturur.
Bazların Genel Özellikleri
- Suda çözündüklerinde suya hidroksit (OH-) iyonu veren maddelere baz adı verilir.
- Tatları acıdır.
- Cildimizde kayganlık hissi oluşturur.
- Bazı metallerle tepkimeye girer ve tepkimeye girdikleri metalleri aşındırır.
- Kırmızı turnusol kâğıdını maviye dönüştürür.
- Sulu çözeltileri elektriği iyi iletir.
- Asitlerle tepkimeye girerek tuz ve su oluşturur.
pH Değeri
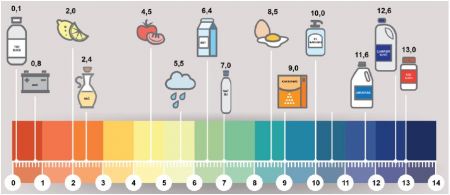
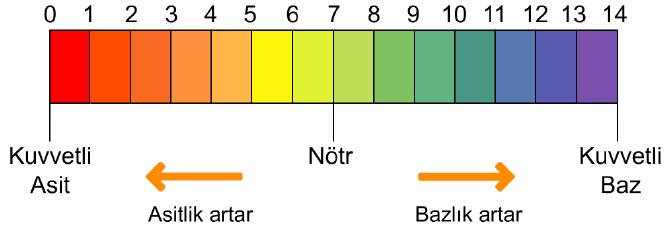
pH değeri, maddelerin asitlik ya da bazlık derecesini gösteren bir ölçüdür. pH değeri, 0 ile 14 arasındaki rakamlarla belirtilir. Bir maddenin pH'si 7'den küçük ise o madde asidik özellik gösterir. pH değeri 7'den 0'a doğru yaklaştıkça maddelerin asidik özelliği artar. Bir maddenin pH'si 7 ise o madde nötrdür; yani ne asidik ne de bazik özellik gösterir. Bir maddenin pH'si 7'den büyük ise o madde bazik özellik gösterir. pH değeri 7'den 14'e doğru yaklaştıkça maddelerin bazik özelliği artar.
Günlük Hayatımızda Asitler ve Bazlar
Günlük hayatımızda tükettiğimiz yiyecekler, içecekler ve kullandığımız temizlik maddeleri farklı asidik ya da bazik özelliğe sahiptir. Akü sıvısı, limon suyu, sirke, domates suyu, yağmur suyu ve süt asidik özellik gösteren maddelerden bazılarıdır. Saf su nötrdür. Kabartma tozu, el sabunu, amonyak ve çamaşır suyu ise bazik özellik gösterir.
Asitler ve bazlar, endüstride çok geniş kullanım alanlarına sahiptir. Hidroklorik asit, nitrik asit ve sülfürik asit endüstride yaygın olarak kullanılan asitlerdendir. Sodyum hidroksit, potasyum hidroksit ve kalsiyum hidroksit ise endüstride yaygın olarak kullanılan bazlardan bazılarıdır.
| Asit ya da Baz Adı | Formülü | Piyasa Adı | Kullanım Alanları |
| Hidroklorik asit | HCI | Tuz ruhu | Kimya, ilaç, petrol, boya ve tekstil endüstrisinde |
| Nitrik asit | HNO3 | Kezzap | Gübre ve boya endüstrisinde, patlayıcı madde üretiminde |
| Sülfürik asit | H2SO4 | Zaç yağı | Gübre ve boya endüstrisinde, patlayıcı madde üretiminde |
| Sodyum hidroksit | NaOH | Sud-kostik | Temizlik, kâğıt, boya ve yapay ipek endüstrisinde |
| Potasyum hidroksit | KOH | Potas-kostik | Sıvı sabun, kâğıt ve tarım ilacı üretiminde |
| Kalsiyum hidroksit | Ca(OH)2 | Sönmüş kireç | Deri, çimento, alçı ve kireç endüstrisinde |
Asit ve Bazlarla Çalışırken Dikkat Edilecek Hususlar
Kuvvetli asit ve bazların canlı ya da cansız maddelere zarar verici etkileri olabilir. Bu nedenle, asitler ve bazlarla çalışırken dikkat etmemiz gereken bazı hususlar vardır.
- Tüm deneylerde olduğu gibi laboratuvarda asitler ve bazlarla çalışırken laboratuvar önlüğü giyilmeli ve laboratuvar gözlüğü takılmalıdır.
- Asitler ve bazlar cildimizi tahriş edebileceği için, asitler ve bazlar ile çalışırken eldiven kullanılmalıdır.
- Kuvvetli asitler ve kuvvetli bazlar koklanmamalı ya da tadına bakılmamalıdır.
- Asit ya da bazların cildimizi tahriş etmesi durumunda en yakın sağlık kuruluşuna başvurulmalıdır.
- Asitler ve bazlar besinlerden uzak bir yerde saklanmalıdır.
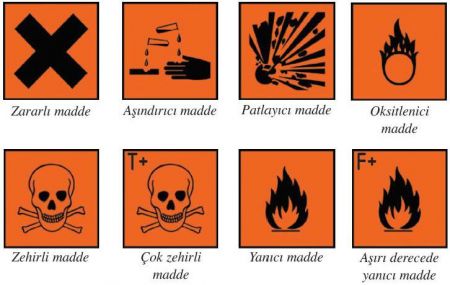
- Asitlerin ve bazların üzerlerindeki tehlike işaretlerine dikkat edilmelidir.
Kaynak: EBA