Sınıf:

Atomun Yapısı
Çevremizdeki bütün maddeler atomlardan oluşmaktadır. Maddenin en küçük yapı taşına atom adı verilmektedir. Maddeleri oluşturan bu atomlar moleküller hâlinde ve birbirine yakın hâlde bulunur. Birbiri ile temas hâlinde olan ve molekülleri oluşturan atomlara ise bağlı atom adı verilir.
Atomu Oluşturan Tanecikler
Bir cam çubuk, ipek kumaşa sürtüldükten sonra kâğıt parçalarına yaklaştırıldığında çubuğun, kâğıt parçalarını çektiği görülür. Bu durum elektriksel çekim kuvveti ile açıklanabilir. Başlangıçta her ikisi de yüksüz olan cam çubuk ve ipek kumaş, sürtme sırasında elektriksel yük kazanmış ve bu yük sayesinde de cam çubuk, kâğıt parçalarını çekebilmiştir. Sürtme sırasında elektriksel yüklerin ortaya çıkması, bu yüklerin en başından beri atomların yapısında bulunduğunu gösterir. Bu da atomların yapısında, atomdan çok daha küçük ve yüklü taneciklerin bulunduğu anlamına gelir. Atomun yapısında bulunan bu taneciklerin bir kısmı pozitif, bir kısmı negatif yüklüdür. Atomun yapısında bulunan pozitif yüklü taneciklere proton, negatif yüklü taneciklere de elektron adı verilir.
Atom, merkezde çekirdek ve çekirdeğin çevresini saran elektronlardan oluşur. Çekirdekte protonlar ve nötronlar vardır. Çekirdekteki yüksüz parçacıklara ise nötron adı verilir. Protonlar pozitif elektrik yüklü, nötronlar ise yüksüzdür. Çekirdeğin çevresinde belirli yörüngelerde sabit hızla hareket eden elektronlar, negatif elektrik yüklüdür.

Protonların ve elektronların elektrik yüklerinin güçleri birbirine eşittir. Buna göre, nötr bir atomda pozitif yüklü protonlar ile negatif yüklü elektronlar birbirini nötrlediği için "Atom yüksüzdür." denir. Örneğin çekirdeğinde 7 proton, 7 nötron ve çekirdeğin çevresinde de 7 elektron bulunduran azot atomunda eşit sayıda pozitif ve negatif yük bulunduğu için nötr hâldedir.
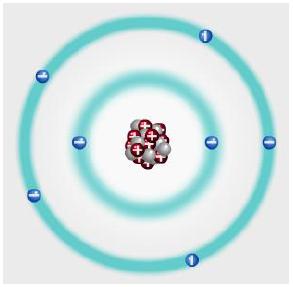
Atomda çekirdekte bulunan pozitif yüklü protonlar ile çekirdeğin çevresinde bulunan negatif yüklü elektronlar arasında bir çekim kuvveti vardır. Çekirdeğe daha yakın olan elektronlara uygulanan çekim kuvveti daha fazladır.
Atom Numarası
Bir atomun çekirdeğinde bulunan protonların sayısı, atomun kimliğini belirler ve bu sayıya atom numarası adı verilir. Örneğin karbon atomunun 6 protonu, azot atomunun 7 protonu, oksijen atomunun ise 8 protonu vardır. Bir elementin atom numarası elementin sembolünün sol altına yazılarak gösterilir. Örneğin atom numarası 13 olan ve Al sembolü ile gösterilen alüminyum elementinin atom numarası 13AI şeklinde gösterilir. Aynı elementin atomları için atom numarası aynı iken nötron sayısı ve elektron sayısı farklılık gösterebilir. Örneğin doğada bulunan karbon atomlarının tamamının çekirdeğinde 6 tane proton bulunurken %98,9'unun nötron sayısı 6, %1,1'inin nötron sayısı 7'dir.
Atom Kütlesi ve Atom Hacmi
Bir elektronun kütlesi, protonun ve nötronun kütlesiyle kıyaslandığında oldukça küçüktür. Yaklaşık olarak 1800 elektronun kütlesi, bir protonun kütlesine eşittir. Buna göre, bir atomun kütlesinin büyük çoğunluğunu çekirdekte bulunan proton ve nötronların kütlesinin oluşturduğu söylenebilir. Bir atomun hacminin büyük çoğunluğunu ise elektronlar oluşturur.
Enerji Katmanı
Elektronlar çekirdeğin çevresinde dairesel yörüngelerde hareket eder. Elektronun bulunma olasılığının fazla olduğu bu yörüngelere katman denir. Çekirdeğe yakın olan katmanda bulunan elektronlar, düşük enerjiye sahipken çekirdekten daha uzakta bulunan elektronlar, daha yüksek enerjiye sahiptir. Her bir katman, belirli sayıda elektron içerir. Birinci katmanda en fazla 2 elektron bulunabilirken, ikinci ve üçüncü katmanlarda en fazla 8 elektron bulunabilir. Bir katman tam olarak elektronla dolu değilken, bir sonraki katmanda elektron bulunamaz.
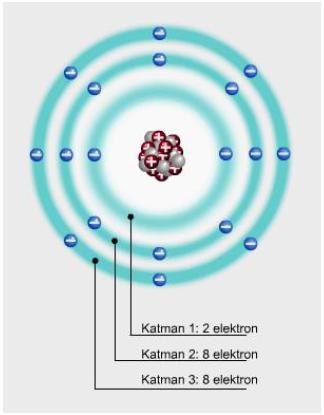
fazla olduğu katmanlar
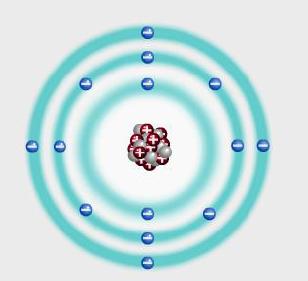
Örneğin çekirdeğinde 14 proton ve 14 nötron bulunan silisyum atomuna ait modelde birinci katmanda 2 elektron, ikinci katmanda 8 elektron ve 3 katmanda da 4 elektron bulunur.
Kaynak: EBA