John Dalton'un Teorisi
Dalton'un atomla ilgili görüşleri şöyle özetlenebilir:1. Elementler atom adı verilen son derece küçük taneciklerden oluşur.2. Belli bir elementin bütün atomları birbirinin aynıdır; yani bu atomların boyutları eşittir, aynı kütleye sahiptir ve kimyasal özellikleri aynıdır. Ancak bir elementin atomları diğer bütün elementlerin atomlarından farklıdır3. Bileşikler birden çok elementin atomlarından oluşmuştur. Herhangi bir bileşikteki iki elementin atom sayılarının oranı bir tam sayı ya da basit tam sayılı bir kesirdir.
4.John Dalton bu teorileri 1803 yılında öne sürdü.
John Josef Thomas'ın Teorisi
Thomson değişik gazlarda yapmış olduğu deneylerle her atomun elektron yükünün kütlesine oranını hesaplayarak elektronu keşfetmiştir. Elektron veren atomun artı (+, pozitif) yüklü olacağını ispatlamış, atom içerisinde proton ve elektronun homojen olarak dağıldığını tanımlamıştır, Bu yüzden bu modele üzümlü kek modeli de denilmektedir. Rutherford Atom Modeli ile proton ve elektronun homojen dağıldığı ilkesi çürütülmüştür
1. Atom artı yüklü maddeden oluşmuştur
2. Elektronlar bu artı madde içinde gömülüdür ve hareket etmezler.
3. Elektronların kütleleri çok küçüktür bu yüzden atomun tüm kütlesini bu artı yüklü madde oluşturur.
4. Atom küre şeklindedir.
5.John Josef bu teorileri 1902 yılında öne sürdü.
Ernest Rutherford'un Teorisi
Rutherford atom modelinin varsayımları şunlardır:
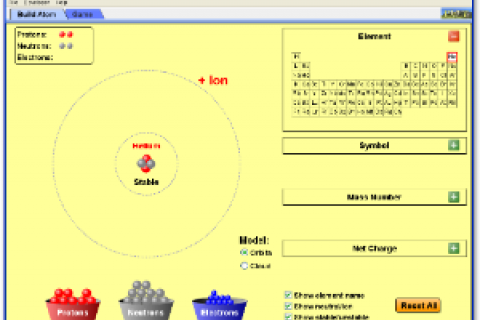
1.Atomda pozitif yük ve kütle, atom merkezinde çekirdek olarak adlandırılan çok küçük bir hacimde toplanmıştır. Atomun yarıçapı 10-10 m, çekirdeğin yarı çapı 10-15 m civarındadır.
2.Çekirdekteki pozitif yük miktarı bir elementin bütün atomları için aynı ve diğer atomlarınkinden farklıdır. Pozitif yük sayısı atom kütlesinin yaklaşık yarısına eşittir.
3.Atomların nötrlüğünü sağlamak üzere, sayısına eşit sayıda elektron, çekirdek etrafında bulunur. Atom hacminin büyük bir bölümü, çok hızlı hareket eden elektronlar tarafından doldurulur.
4.Ernest bu teorileri 1911 yılında öne sürdü
Riheles David Borh'un Teorisi
Bohr atom modelinin varsayımları şunlardır:
Elektronlar çekirdek çevresinde yarı çapı belli dairesel yörüngelerde bulunabilir. Bu yörüngelere enerji düzeyi de denir. Yörüngeler çekirdeğe yakınlık sırasına göre ya K, L, M… gibi harflerle, ya da 1, 2, 3, …n gibi tam sayılarla gösterilir. Her enerji düzeyinin belirli bir enerjisi vardır.
Çekirdeğe en yakın enerji seviyesinin enerjisi en küçüktür. Çekirdekten uzaklaştıkça yörüngelerin enerjisi artar. Hidrojen atomunda bir elektron en düşük enerjili yörüngede bulunur. Bu yörüngelerden birinde bulunan elektron kendiliğinden enerji yaymaz. Elektronu olası en düşük enerjili yörüngelerde bulunan atomun elektron dizilişine temel hal elektron dizilişi denir. Atom dışarıdan enerji kazanırsa elektron aldığı enerjinin değerine bağlı olarak daha yüksek enerjili bir düzeye sıçrar. Böyle elektronlara uyarılmış elektron, atomlara da uyarılmış atom denir.
Uyarılmış elektron, daha düşük enerjili bir düzeye düşerken hareket ettiği iki enerji düzeyi farkına eşit enerjiyi dışarıya verir
Borh bu teorileri 1927 yılında öne sürdü.
Marie Curie'nin Teorisi
Dalton’dan sonra atom konusunda çalışmalar devam etmiştir.Atomu zorda olsa bölünebildiğini ve atomdan daha küçük parçaların da bulunduğu Dalton’tan 50 yıl sonra kanıtlanmıştır.Atomların bölünebildiğini Marie Curie (Meri Küri) ve Henry ßecqueret (Henri Bekerel) gibi bilim insanlarının çalışmalarıyla ispatlanmıştır
Kaynakça
http://www.odevsel.com/bilim/1939/atom-modelleri-ve-modern-atom-teorisi....
Fen Ve Teknolojı Ders Kitabı Sayfa 93
http://www.dersdoktoru.com/default.asp?sayfala=ders_sunusu_goster&id=57